양성자펌프억제제가 수면무호흡증 환자에게 미치는
영향
 0
양산부산대학교병원 박지환
0
양산부산대학교병원 박지환

서론
폐쇄성 수면무호흡증(Obstructive Sleep Apnea, OSA)은 수면 중 반복되는 상기도의 협착이나 폐쇄로 인해 무호흡과 저호흡이 발생하는 질환으로, 고혈압, 뇌혈관 질환, 당뇨병, 우울증 등 다양한 합병증을 야기할 수 있다. 최근 연구들은 OSA와 위식도역류질환(gastroesophageal reflux disease, GERD) 및 인후두역류(laryngopharyngeal reflux, LPR)와 같은 역류성 질환이 OSA와 밀접한 연관성을 가진다는 점을 보고해 왔다. OSA 환자의 54~76%에서 GERD가 동반되는 것으로 보고되고[1, 2], 이는 일반 인구 집단에서의 GERD 유병률보다 현저히 높은 수치이다. OSA와 위식도역류질환(gastroesophageal reflux disease, GERD)은 상호 밀접한 관련성을 가진 질환으로, 각각의 질환이 서로의 발병 및 경과에 영향을 미치는 것으로 보인다. 양성자펌프억제제(proton pump inhibitor, PPI)는 GERD의 표준 치료법으로 널리 사용되고 있으며, 최근 연구들에서는 PPI 치료가 동반된 GERD를 가진 OSA 환자에서 수면 관련 증상 개선에 기여할 가능성도 제시되고 있다.
OSA와 GERD의 병태생리학적 연관성
OSA와 GERD 간의 연관성은 여러 기전을 통해 설명될 수 있다. 첫째, OSA에서 나타나는 반복적인 상부기도 폐쇄는 흉강 내 음압을 증가시켜 위식도역류를 촉진한다. 무호흡 발작 시 발생하는 강한 흉곽 내 음압은 하부식도괄약근의 일시적 이완을 유발하여 위 내용물의 역류를 촉진하는 주요한 요인으로 작용할 수 있다. 둘째, 역류된 위산이 상부 기도에 도달하여 후두와 인두 점막에 염증과 부종을 유발함으로써 기도 개방성을 저해하고 OSA를 악화시킬 수도 있다. 특히 인후두역류는 성대나 상부 기도 주변 연조직의 두께를 증가시켜 기도 협착을 유발할 수 있으며, 미주신경 자극을 통한 기관지 수축으로 인해 코골이나 OSA를 야기할 수 있다. 셋째, 인후두역류로 인해 위산이 인두와 후두 점막에 지속적으로 노출되면 해당 부위의 감각신경 역치가 변화하고, 반사적 기도 수축이 항진된다. 이 과정에서 상부기도 확장근 (pharyngeal dilator muscle)의 반사 기능을 저하시켜 결과적으로 기도 개방성이 감소하여 OSA를 더욱 악화시키는 악순환 구조가 형성된다. 마지막으로, 수면 중에는 연하, 타액 분비, 식도 일차 운동성 등 산의 청소 기전이 저하되어 역류된 위산의 접촉 시간이 연장되어 GERD를 더욱 악화시킬 수 있다[3].
PPI 치료가 OSA에 미치는 효과에 대한 임상적 근거
메타분석 결과 및 주요 연구Rassameehiran 등이 수행한 체계적 문헌고찰 및 메타분석에서는 GERD를 동반한 OSA 환자에서 PPI 치료의 효과를 평가하였다. 무호흡-저호흡지수(apnea-hypopnea index, AHI)에 대한 분석에서는 PPI 치료 전후 유의한 차이가 관찰되지 않았으나 2개의 코호트 연구에서는 무호흡지수가 유의하게 감소하였으며(31%와 35%의 개선), 한 연구에서는 무호흡 발작의 빈도가 73% 감소하는 것으로 나타났다. 주간 졸림증을 평가하는 Epworth 졸음척도(Epworth Sleepiness Scale, ESS)에서는 3개의 코호트 연구와 1개의 임상시험에서 유의한 개선이 관찰되었다[4]. Suurna 등의 이중맹검, 무작위, 위약대조 교차시험에서는 pantoprazole 40mg을 투여받은 군에서 ESS가 유의하게 감소하였다(p=0.04)[5].
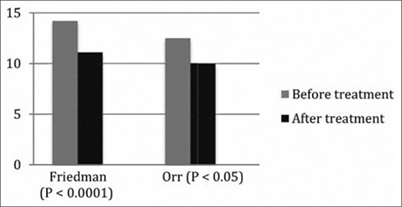 Figure 1. PPI 치료가 Epworth 졸음척도에 미치는 효과 (figure from Rassameehiran et al., 2016)
Figure 1. PPI 치료가 Epworth 졸음척도에 미치는 효과 (figure from Rassameehiran et al., 2016)
소아 OSA 환자를 대상으로 한 연구에서는 조금 더 뚜렷한 효과가 관찰되었다. Wasilewska 등의 연구에서는 GERD 증상을 동반한 37명의 OSA 소아 환자에게 4~8주간 omeprazole 치료(1mg/kg)를 시행한 결과, AHI가 13.08±3.11/h에서 8.22±2.52/h로 유의하게 감소하였다(p<0.01). 특히 경미한 OSA 환자 3명에서는 완전한 호전이 관찰되었으며, 중증 OSA 환자에서는 상대적으로 제한적인 반응을 보였다[6].
예측 인자 및 반응성Modolell 등의 연구에서는 199명의 수면호흡장애 환자를 대상으로 pantoprazole 치료의 예측 인자를 분석하였다. 치료 전 근위부 식도 pH 검사에서 병리적 소견을 보인 환자의 67%에서 임상적 또는 수면다원검사상 호전을 보였고, 근위부 식도 역류가 PPI 치료 반응의 중요한 예측 인자임을 시사하였다[7].
OSA에서 PPI의 작용 기전
PPI는 H+-K+-ATPase를 억제하여 위산분비를 감소시키고, pepsin 활성도를 저하시키며, 염증반응을 차단하는 기전을 통해 작용한다. OSA와 관련하여서는 다음과 같은 치료적 효과를 기대할 수 있다. 첫째, 위산분비 억제를 통한 직접적인 역류 감소 효과이다. 위산량의 감소는 역류 발생 빈도와 강도를 줄여 상부기도 점막의 산 노출을 최소화한다. 둘째, 상부 기도 염증의 감소이다. 후두인두역류로 인한 만성 염증과 부종이 감소함에 따라 상부기도의 해부학적 협착이 개선될 수 있다. 셋째, 감각 기능의 회복이다. 산으로 인한 후두 점막의 감각 손상이 회복됨에 따라 상부기도 확장근의 반사 기능이 정상화될 수 있다. 그러나 PPI 치료가 해부학적 변화로 인한 산-역류 관련 손상을 완전히 회복시키기 위해서는 최대 6개월의 치료 기간이 필요할 수 있으며, 대부분의 연구에서는 이보다 짧은 치료 기간을 적용했다는 한계가 있다[8].
OSA에서 PPI의 임상적 적용
현재까지의 근거를 바탕으로 할 때, PPI 치료는 다음과 같은 OSA 환자에서 우선적으로 고려될 수 있다. 우선 GERD나 LPR 증상을 동반한 OSA 환자에서는 반드시 PPI 치료를 고려해야 한다. 이는 역류 증상 치료를 위한 것이며, 수면의 질 개선은 부가적 효과로 기대할 수 있다. 그리고 주간 과다졸림증이 현저한 환자에서는 CPAP 치료와 병행하여 PPI 치료를 시도해 볼 수 있다. 특히 ESS 점수가 높은 환자에서 증상 개선을 기대할 수 있다. 그리고 24시간 pH 검사에서 근위부 식도 역류가 확인된 환자의 경우에는 PPI 치료에 대한 반응성이 좀 더 높을 것으로 예상해 볼 수 있다.
CPAP 치료는 그 자체로서 야간 위식도역류 증상을 감소시키는 효과가 있는 것으로 알려져 있다[2]. 양압이 위식도접합부의 압력을 변화시켜 역류를 감소시키고, 식도 운동성을 개선하여 식도 청소 기능을 향상시킬 수 있다[9]. 따라서 중등도 이상의 OSA 환자에서는 CPAP 치료를 우선적으로 시행하고, GERD나 LPR 증상이 지속되는 경우에 PPI를 추가하는 것을 고려해 볼 수 있겠다.
향후 연구 방향 및 결론
PPI와 OSA의 관계에 대한 보다 확실한 근거를 확립하기 위해서는 다음과 같은 연구가 필요하다. 우선 대규모 무작위대조시험을 통한 PPI의 OSA에 대한 효과 검증이 필요하다. 특히 AHI와 같은 객관적 지표에 대한 효과를 명확히 규명해야 한다. 그리고 최적의 치료 기간과 용량을 결정하기 위한 용량-반응 관계 연구가 요구된다. 현재 대부분의 연구가 6~8주의 단기간 치료 결과이므로, 장기간 치료의 효과와 안전성에 대한 평가가 필요할 것으로 생각한다. 그뿐만 아니라 PPI 치료 반응을 예측할 수 있는 바이오마커나 임상적 지표의 개발도 중요하며 24시간 pH 검사 외에도 보다 간편하고 실용적인 예측 도구가 필요하다. 또한 연령층, 비만도, OSA 중증도에 따른 차별적 치료 전략 개발이 필요하고, 특히 소아에서 관찰된 뚜렷한 효과가 성인에서도 재현될 수 있는지에 대한 추가 연구가 요구된다[6, 10].
결론
결론적으로, 현재까지의 연구들은 GERD를 동반한 OSA 환자에서 PPI 치료가 AHI에는 유의한 영향을 미치지 않지만, 주간 졸림증과 수면의 질 개선에는 도움이 될 수 있음을 시사한다. 이비인후과 의사들은 OSA 환자에서 동반된 GERD나 LPR 증상이 있는 경우 적극적인 PPI 치료를 고려해야 하며, 이를 통해 역류 증상 개선뿐만 아니라 수면 관련 증상의 부가적 개선 효과를 기대할 수 있다. 그러나 PPI 치료만으로는 OSA의 근본적인 해결책이 될 수 없으므로, CPAP 등의 표준 치료와 병행하는 종합적 접근이 필요하다.
References
- Ing AJ, Ngu MC, Breslin AB. Obstructive sleep apnea and gastroesophageal reflux. Am J Med 2000;108(Suppl 4a):120S-125S.
- Green BT, Broughton WA, O'Connor JB. Marked improvement in nocturnal gastroesophageal reflux in a large cohort of patients with obstructive sleep apnea treated with continuous positive airway pressure. Arch Intern Med 2003;163(1):41-45.
- Fass R, Quan SF, O'Connor GT, Ervin A, Iber C. Predictors of heartburn during sleep in a large prospective cohort study. Chest 2005;127(5):1658-1666.
- Rassameehiran S, Klomjit S, Hosiriluck N, Nugent K. Meta-analysis of the effect of proton pump inhibitors on obstructive sleep apnea symptoms and indices in patients with gastroesophageal reflux disease. Proc (Bayl Univ Med Cent) 2016;29(1):3-6.
- Suurna MV, Welge J, Surdulescu V, Kushner J, Steward DL. Randomized placebo-controlled trial of pantoprazole for daytime sleepiness in GERD and obstructive sleep disordered breathing. Otolaryngol Head Neck Surg 2008;139(2):286-290.
- Wasilewska J, Semeniuk J, Cudowska B, Klukowski M, Dębkowska K, Kaczmarski M. Respiratory response to proton pump inhibitor treatment in children with obstructive sleep apnea syndrome and gastroesophageal reflux disease. Sleep Med 2012;13(7):824-830.
- Modolell I, Esteller E, Segarra F, Mearin F. Proton-pump inhibitors in sleep-related breathing disorders: clinical response and predictive factors. Eur J Gastroenterol Hepatol 2011;23(10):852-858.
- Friedman M, Gurpinar B, Lin HC, Schalch P, Joseph NJ. Impact of treatment of gastroesophageal reflux on obstructive sleep apnea-hypopnea syndrome. Ann Otol Rhinol Laryngol 2007;116(11):805-811.
- Kuribayashi S, Kusano M, Kawamura O, Shimoyama Y, Maeda M, Hisada T, Ishizuka T, Dobashi K, Mori M. Mechanism of gastroesophageal reflux in patients with obstructive sleep apnea syndrome. J Gastroenterol 2010;45(12):1219-1227.
- He J, Wang C, Li W. Laryngopharyngeal Reflux in Obstructive Sleep Apnea-Hypopnea Syndrome: An Updated Meta-Analysis. Nat Sci Sleep 2022;14:2189-2201.




